Termodynamikken til materiens gassformige aggregattilstand er en viktig gren av fysikken som studerer termodynamisk likevekt og kvasi-statiske overganger i systemer. Hovedmodellen som prediksjoner av systemenes oppførsel er basert på er den ideelle gassmodellen. Med bruken ble Mendeleev-Clapeyron-ligningen oppnådd. Tenk på det i artikkelen.
Ideell gass
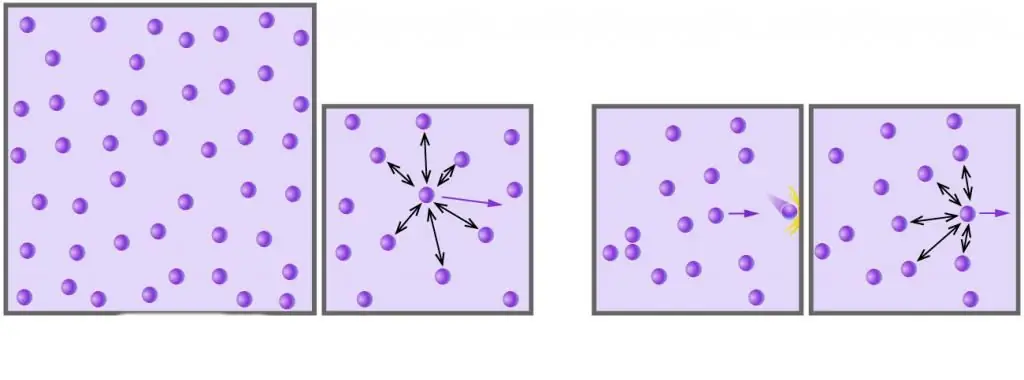
Som du vet, består alle ekte gasser av molekyler eller atomer, avstandene mellom dem er for store sammenlignet med størrelsen ved lavt trykk. I tillegg, ved høye temperaturer, i en absolutt skala, overstiger den kinetiske energien til molekyler deres potensielle energi assosiert med svake dipol-dipol-interaksjoner (hvis det i tillegg til disse interaksjonene er andre typer kjemiske bindinger, for eksempel ioniske eller hydrogen, så gir de et betydelig bidrag til den potensielle komponenten i den interne systemenergien).
På grunn avFor mange virkelige gasser under forhold nær det normale, kan man neglisjere deres indre interaksjoner og partikkelstørrelser. Disse to hovedtilnærmingene utgjør den ideelle gassmodellen.
Mendeleevs ligning i fysikk

Det er mer riktig og rettferdig å kalle denne ligningen Clapeyron-Mendeleev-loven. Faktum er at det først ble spilt inn av den franske ingeniøren Emile Clapeyron i 1834. Han gjorde dette ved å analysere gasslovene til Boyle-Mariotte, Gay-Lussac og Charles som ble oppdaget på begynnelsen av 1800-tallet.
Fortjenesten til den russiske kjemikeren Dmitrij Mendeleev ligger i det faktum at han ga ligningen en moderne og lettbrukt matematisk form. Spesielt introduserte Mendeleev i ligningen en konstant for alle gasser R=8, 314 J/(molK). Clapeyron brukte selv en rekke empiriske konstanter som gjør beregningsprosessen vanskelig.
Mendeleev-Clapeyron-ligningen er skrevet som følger:
PV=nRT.
Denne likheten betyr at produktet av trykk P og volum V på venstre side av uttrykket alltid er proporsjon alt med produktet av absolutt temperatur T og mengden av stoff n på venstre side.
Uttrykket som studeres lar deg få en hvilken som helst gasslov hvis du fikser to av de fire parameterne. Ved isoprosesser studeres lukkede systemer der det ikke er utveksling av materie med omgivelsene (n=const). Disse prosessene er preget av en enkelt fast termodynamisk parameter (T, P eller V).

Eksempelproblem
La oss nå løse problemet med Mendeleev-Clapeyron-ligningen. Det er kjent at oksygen som veier 500 gram er i en sylinder med et volum på 100 liter ved et trykk på 2 atmosfærer. Hva er temperaturen i ballongen, gitt at systemet er i termodynamisk likevekt.
Husk at mengden av et stoff ifølge definisjonen beregnes ved hjelp av formelen:
n=m/M.
Der m er massen til alle partikler i systemet, er M deres gjennomsnittlige molare masse. Denne likheten lar oss omskrive Mendeleev-ligningen i følgende form:
PV=mRT/M.
Hvor får vi arbeidsformelen for denne oppgaven:
T=PVM/(mR).
Det gjenstår å konvertere alle mengder til SI-enheter og erstatte dem med dette uttrykket:
T=21013250, 10, 032/(0, 58, 314)=156 K.
Beregnet temperatur er -117 oC. Selv om oksygen ved denne temperaturen fortsatt er gassformig (det kondenserer ved -182,96 oC), kan den ideelle gassmodellen under slike forhold bare brukes til å oppnå et kvalitativt estimat av den beregnede verdien.






