Molekylær-kinetisk teori tillater, ved å analysere den mikroskopiske oppførselen til systemet og bruke metodene for statistisk mekanikk, å oppnå viktige makroskopiske egenskaper ved det termodynamiske systemet. En av de mikroskopiske egenskapene, som er relatert til temperaturen i systemet, er den gjennomsnittlige kvadrathastigheten til gassmolekyler. Vi gir formelen for det og vurderer det i artikkelen.
Ideell gass
Vi merker umiddelbart at formelen for den kvadratiske gjennomsnittshastigheten til gassmolekyler vil bli gitt spesifikt for en ideell gass. Under det, i fysikk, vurderes et slikt mangepartikkelsystem der partikler (atomer, molekyler) ikke samhandler med hverandre (deres kinetiske energi overstiger den potensielle energien for interaksjon med flere størrelsesordener) og ikke har dimensjoner, det vil si at de er punkter med en endelig masse (avstanden mellom partiklene som er flere størrelsesordener større enn deres størrelse.lineær).
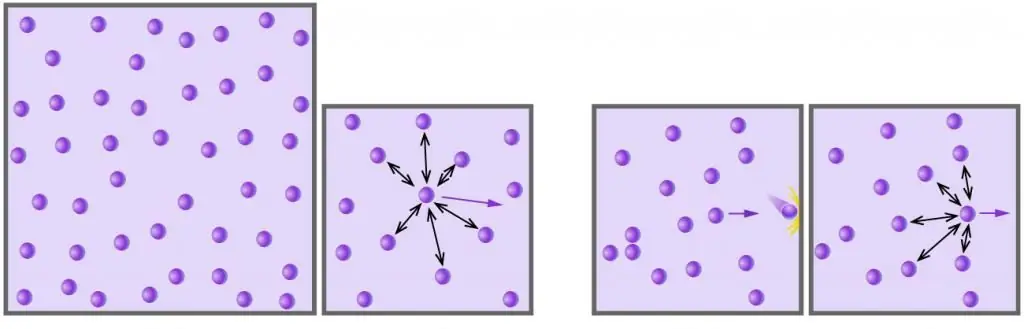
Enhver gass som består av kjemisk nøytrale molekyler eller atomer, og som er under lavt trykk og har høy temperatur, kan betraktes som ideell. For eksempel er luft en ideell gass, men vanndamp er ikke lenger slik (sterke hydrogenbindinger virker mellom vannmolekyler).
Molecular Kinetic Theory (MKT)

Når du studerer en ideell gass innenfor rammen av MKT, bør du være oppmerksom på to viktige prosesser:
- Gass skaper trykk ved å overføre til veggene i karet som inneholder den, momentumet når molekyler og atomer kolliderer med dem. Slike kollisjoner er perfekt elastiske.
- Molekyler og gassatomer beveger seg tilfeldig i alle retninger med forskjellige hastigheter, fordelingen av disse følger Maxwell-Boltzmann-statistikken. Sannsynligheten for kollisjon mellom partikler er ekstremt lav, på grunn av deres ubetydelige størrelse og store avstander mellom dem.
Til tross for at de individuelle hastighetene til gasspartikler er svært forskjellige fra hverandre, forblir gjennomsnittsverdien av denne verdien konstant over tid hvis det ikke er ytre påvirkninger på systemet. Formelen for gjennomsnittlig kvadrathastighet til gassmolekyler kan fås ved å vurdere forholdet mellom kinetisk energi og temperatur. Vi vil behandle dette problemet i neste avsnitt av artikkelen.
Derivering av formelen for den kvadratiske gjennomsnittshastigheten til ideelle gassmolekyler
Enhver student vet fra det generelle kurset i fysikk at den kinetiske energien til translasjonsbevegelsen til et legeme med masse m beregnes som følger:
Ek=mv2/2
Hvor v er den lineære hastigheten. På den annen side kan den kinetiske energien til en partikkel også bestemmes ut fra den absolutte temperaturen T, ved å bruke konverteringsfaktoren kB(Boltzmanns konstant). Siden rommet vårt er tredimensjon alt, beregnes Ek som følger:
Ek=3/2kBT.
Tilsvarer begge likheter og uttrykker v fra dem, får vi formelen for gjennomsnittshastigheten til en kvadratisk idealgass:
mv2/2=3/2kBT=>
v=√(3kBT/m).
I denne formelen er m - massen til gasspartikkelen. Verdien er upraktisk å bruke i praktiske beregninger, siden den er liten (≈ 10-27kg). For å unngå denne ulempen, la oss huske den universelle gasskonstanten R og den molare massen M. Konstanten R med kB er relatert med likheten:
kB=R/NA.
Verdien av M er definert som følger:
M=mNA.
Ta hensyn til begge likhetene, får vi følgende uttrykk for rot-middelkvadrathastigheten til molekyler:
v=√(3RT/M).
Den gjennomsnittlige kvadrathastigheten til gasspartikler er direkte proporsjonal med kvadratroten av absolutt temperatur og omvendt proporsjonal med kvadratroten av molar masse.
Eksempel på problemløsning
Alle vet at luften vi puster inn består av 99 % nitrogen og oksygen. Det er nødvendig å bestemme forskjellene i gjennomsnittshastighetene til molekylene N2 og O2 ved en temperatur på 15 o C.

Dette problemet vil bli løst sekvensielt. Først oversetter vi temperaturen til absolutte enheter, vi har:
T=273, 15 + 15=288, 15 K.
Skriv nå ut molarmassene for hvert molekyl som vurderes:
MN2=0,028 kg/mol;
MO2=0,032 kg/mol.
Siden verdiene av molarmasser avviker litt, bør gjennomsnittshastighetene deres ved samme temperatur også være nærme. Ved å bruke formelen for v får vi følgende verdier for nitrogen- og oksygenmolekyler:
v (N2)=√(38, 314288, 15/0, 028)=506,6 m/s;
v (O2)=√(38, 314288, 15/0, 032)=473,9 m/s.
Fordi nitrogenmolekyler er litt lettere enn oksygenmolekyler, beveger de seg raskere. Gjennomsnittlig hastighetsforskjell er:
v (N2) - v (O2)=506,6 - 473,9=32,7 m/ s.
Den resulterende verdien er bare 6,5 % av gjennomsnittshastigheten til nitrogenmolekyler. Vi gjør oppmerksom på de høye hastighetene til molekyler i gasser, selv ved lave temperaturer.






