Kunnskap om definisjoner i fysikk er en nøkkelfaktor for å lykkes med å løse ulike fysiske problemer. I artikkelen vil vi vurdere hva som menes med isobariske, isokoriske, isotermiske og adiabatiske prosesser for et ideelt gasssystem.
Ideell gass og dens ligning
Før vi går videre til beskrivelsen av isobariske, isokoriske og isotermiske prosesser, la oss vurdere hva en ideell gass er. Under denne definisjonen i fysikk anser de et system som består av et stort antall dimensjonsløse og ikke-samvirkende partikler som beveger seg med høy hastighet i alle retninger. Faktisk snakker vi om en gassformig aggregert tilstand av materie, der avstandene mellom atomer og molekyler langt overstiger størrelsen deres, og der den potensielle energien for interaksjon av partikler blir neglisjert på grunn av dens litenhet, sammenlignet med den kinetiske energien.
Tilstanden til en ideell gass er totalen av dens termodynamiske parametere. De viktigste er temperatur, volum og trykk. La oss betegne dem med henholdsvis bokstavene T, V og P. På 30-tallet av XIX århundreClapeyron (en fransk vitenskapsmann) skrev først ned en ligning som kombinerer de angitte termodynamiske parameterne innenfor en enkelt likhet. Det ser ut som:
PV=nRT,
hvor n og R er henholdsvis mengden av stoffer og gasskonstanten.
Hva er isoprosesser i gasser?
Som mange har lagt merke til, bruker isobariske, isokoriske og isotermiske prosesser det samme "iso"-prefikset i navnene sine. Det betyr likheten til én termodynamisk parameter under gjennomgangen av hele prosessen, mens de resterende parameterne endres. For eksempel indikerer en isoterm prosess at som et resultat holdes den absolutte temperaturen i systemet konstant, mens en isokorisk prosess indikerer et konstant volum.
Isoprosesser er praktiske å studere, siden fiksering av en av de termodynamiske parameterne fører til en forenkling av den generelle ligningen for gasstilstand. Det er viktig å merke seg at gasslovene for alle disse isoprosessene ble oppdaget eksperimentelt. Analysen deres tillot Clapeyron å oppnå den reduserte universelle ligningen.
Isobariske, isokoriske og isotermiske prosesser
Den første loven ble oppdaget for en isoterm prosess i en ideell gass. Nå heter den Boyle-Mariotte-loven. Siden T ikke endres, innebærer tilstandsligningen likheten:
PV=const.
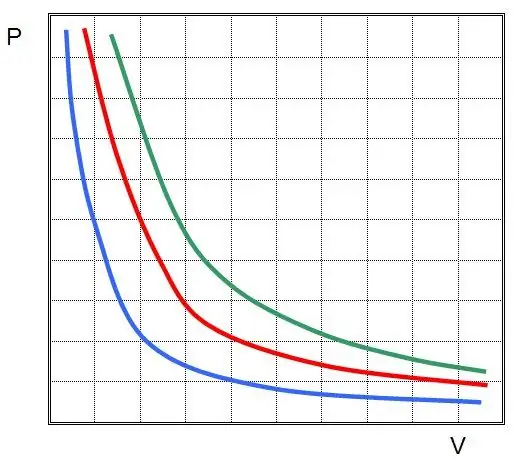
Med andre ord fører enhver trykkendring i systemet til en omvendt proporsjonal endring i volumet, hvis temperaturen på gassen holdes konstant. Grafen til funksjonen P(V) erhyperbole.
Isobarisk prosess - dette er en endring i systemets tilstand, der trykket forblir konstant. Etter å ha fastsatt verdien av P i Clapeyron-ligningen, får vi følgende lov:
V/T=const.
Denne likheten bærer navnet til den franske fysikeren Jacques Charles, som mottok den på slutten av 1700-tallet. Isobaren (grafisk representasjon av V(T)-funksjonen) ser ut som en rett linje. Jo mer trykk i systemet, jo raskere stiger denne linjen.
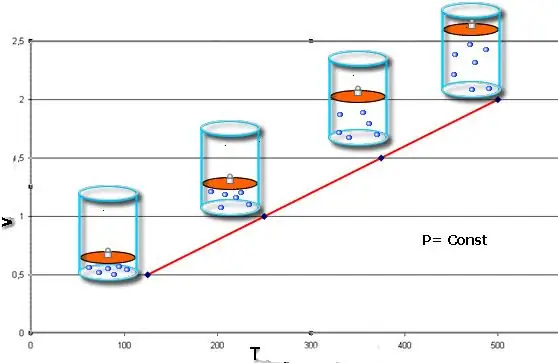
Den isobariske prosessen er enkel å implementere hvis gassen varmes opp under stempelet. Molekylene til sistnevnte øker hastigheten (kinetisk energi), skaper et høyere trykk på stempelet, noe som fører til utvidelse av gassen og opprettholder en konstant verdi på P.
Til slutt er den tredje isoprosessen isokorisk. Den kjører med konstant volum. Fra tilstandsligningen får vi den tilsvarende likheten:
P/T=konstant.
Det er kjent blant fysikere som Gay-Lussacs lov. Den direkte proporsjonaliteten mellom trykk og absolutt temperatur indikerer at grafen for den isobare prosessen, i likhet med grafen til den isobare, er en rett linje med positiv helning.
Det er viktig å forstå at alle isoprosesser forekommer i lukkede systemer, det vil si at verdien av n blir bevart i løpet av deres forløp.
Adiabatisk prosess
Denne prosessen tilhører ikke "iso"-kategorien, siden alle de tre termodynamiske parameterne endres under gjennomgangen. adiabatiskk alt overgangen mellom to tilstander i systemet, der det ikke utveksler varme med omgivelsene. Dermed utføres utvidelsen av systemet på grunn av dets interne energireserver, noe som fører til et betydelig fall i trykk og absolutt temperatur i det.
Adiabatisk prosess for en ideell gass er beskrevet av Poissons ligninger. En av dem er vist nedenfor:
PVγ=const,
der γ er forholdet mellom varmekapasiteter ved konstant trykk og ved konstant volum.
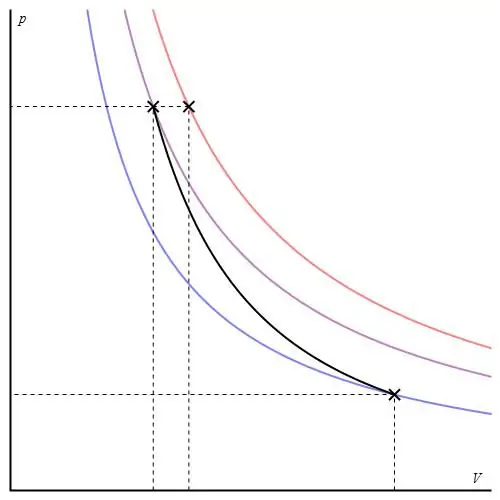
Den adiabatiske grafen skiller seg fra den isokoriske prosessgrafen og fra den isobariske grafen, men den ligner på en hyperbel (isoterm). Adiabaten i P-V-aksene oppfører seg skarpere enn isotermen.






